OSTEOGENESIS IMPERFECTA: ANESTHETIC MANAGEMENT OF A PATIENT WITH A FEMORAL FRACTURE. CASE REPORT
RESUMEN
Introducción. La osteogénesis imperfecta es una enfermedad congénita rara del tejido conectivo, con mayor incidencia en mujeres. Puede ser causada por mutación en uno de los genes que codifican el colágeno, proteínas involucradas en la modificación postraduccional o el procesamiento del mismo, así como defectos de diferenciación y función de osteoblastos. Sus manifestaciones clínicas incluyen la susceptibilidad a las fracturas óseas y retraso del crecimiento, así como compromiso del tejido conectivo de otros órganos, con morbimortalidad variable.
Caso Clínico. Paciente masculino de 25 años con diagnóstico de osteogénesis imperfecta y antecedente de fracturas de repetición que ingresa para tratamiento de osteosíntesis por fractura de fémur izquierdo.
Conclusión. En la práctica de la anestesia, el anestesiólogo se encuentra con pacientes con enfermedades congénitas raras que representan un desafío debido a complicaciones asociadas con la enfermedad.
Palabras Clave: Osteogénesis Imperfecta; Enfermedad de Huesos Frágiles; Colágeno tipo I; Anestesia.
ABSTRACT
Introduction. Osteogenesis imperfecta is a rare congenital disease of connective tissue, with a higher incidence in women. It can be caused by mutation in one of the genes that encode collagen, proteins involved in post-translational modification or collagen processing, as well as osteoblast differentiation and function defects. Its clinical manifestations include susceptibility to bone fractures and growth retardation, as well as the compromise of the connective tissue of other organs, with variable morbidity and mortality.
Clinical case. 25-year-old male patient with a diagnosis of osteogenesis imperfecta and a history of recurrent fractures admitted to the treatment of osteosynthesis due to a left femur fracture.
Conclusion. In the practice of anesthesia, the anesthesiologist encounters patients with rare congenital diseases that represent a challenge due to complications associated with the disease.
Keywords: Osteogenesis Imperfecta; Fragile Bone Disease; Type I collagen; Anesthesia.
INTRODUCCIÓN
La Osteogénesis imperfecta (OI) es una displasia esquelética hereditaria, que comparte una etiología relacionada con el colágeno tipo I, presenta una incidencia de 1/10000-25000 nacimientos en el mundo (1,2). Las características clínicas más comunes incluyen fragilidad y deformidad ósea, así como deficiencia en el crecimiento. Los síntomas variables adicionales asociados incluyen esclerótica azul, pérdida auditiva, dentinogénesis imperfecta, hipercalciuria, deficiencia en las capacidades pulmonares, disfunción valvular cardíaca, siendo la insuficiencia aórtica la más frecuente, seguido del prolapso de la válvula mitral y disección de aorta (1,2,7).
La clasificación de Sillence original (tipos I-IV), que precedió a la identificación de las causas moleculares de la OI, se basa en criterios genéticos, mutaciones autosómicas dominantes en COL1A1 o COL1A2, que alteran directamente la cantidad o la estructura primaria del colágeno tipo I, dando las características radiológicas y clínicas (1-5). La comprensión de la OI como un trastorno relacionado con el colágeno ha permitido una descripción más específica de la OI en 18 subtipos funcionalmente relacionados según las características clínicas, la histología ósea, los patrones de herencia y las causas genéticas. La OI ahora se clasifica según las distinciones histológicas y las características fenotípicas (tipos V y VI), los patrones de herencia autosómica recesiva de mutaciones en genes que codifican proteínas involucradas en la modificación postraduccional (tipo VII-IX) o el procesamiento y la reticulación (tipos X-XII) de colágeno y defectos de diferenciación y función de osteoblastos (tipos XIII-XVIII) (1, 2, 6, 7).
La gravedad fenotípica es extremadamente variable, oscila desde la letalidad en el período perinatal hasta los casos más leves que se presentan como una condición osteoporótica (1,8-10).
Los pacientes afectados tienen múltiples fracturas desde la infancia, tanto traumatismo espontáneo como fracturas relacionadas con un mínimo esfuerzo físico (2-4). El 65% de las fracturas en estos pacientes se encuentran en miembros inferiores (2,5,6).
El diagnóstico de esta enfermedad es básicamente clínico, en función a los hallazgos, perinatales y postnatales del individuo. Radiográficamente se determinará la disminución en la densidad y matriz mineral de los huesos, múltiples fracturas, presencia de matrices exuberantes y alteraciones metafisiarias. La biopsia de tejido epitelial y ósea, acompañado de cultivos de fibroblastos ayudará al diagnóstico (6).
La prevención de las fracturas es el manejo más apropiado, apoyado con terapia física y soportes óseos. El manejo quirúrgico solamente está indicado en la reparación de las lesiones o la corrección de las mismas, apoyado con el uso de medicamentos que fortalezcan la matriz ósea, como la hormona de crecimiento o bifosfonatos (6). Las fracturas desplazadas deben ser cuidadosamente alineadas y enyesadas, diversos estudios indican que el índice de migración de clavos y re fractura es alto (2,5,6).
En caso de intervención quirúrgica de un paciente con OI, la preparación adecuada y la evaluación preoperatoria son importantes, como es la elección de la técnica anestésica, la correcta identificación de factores de riesgo y la optimización de la salud antes de la cirugía (7).
CASO CLÍNICO
Paciente masculino de 25 años de edad, peso 60 kg, estatura 1.55 m, peso ideal 52.9-26 kg, peso corregido 54.7 kg. Sin antecedentes heredofamiliares de relevancia. Diagnóstico de osteogénesis imperfecta realizado a los 10 meses de edad por historial de fracturas de repetición y estudios radiográficos. Refiere diecisiete fracturas previas, de las cuales dos necesitaron de abordaje quirúrgico a los 7 y 11 años de edad respectivamente, ambos eventos bajo anestesia general, sin complicaciones aparentes.
Presenta caída de su propia altura, datos clínicos y radiográficos indicativos de fractura de fémur izquierdo, programado para osteosíntesis de forma electiva. En la valoración anestésica no refiere otro antecedente patológico de importancia.
Figura 1. Radiografía AP de miembro pélvico izquierdo, se muestra fractura y alteración en la densidad del hueso.
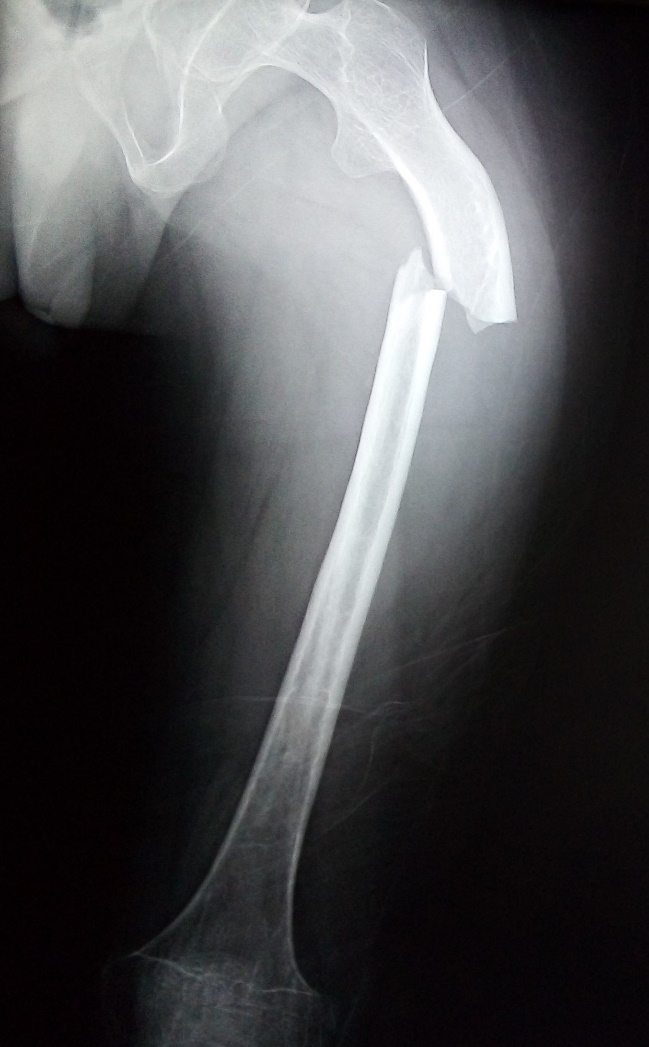
Examen físico: signos vitales dentro de parámetros normales. Cara en forma triangular, escleras blancas, limitación a la flexo extensión de cuello, escoliosis dorso lumbar, tórax en tonel, amplexión y amplexación disminuidas, ruidos cardiacos rítmicos, de buena intensidad y frecuencia, abdomen blando, depresible, no doloroso, curvatura anormal en extremidades superiores, cicatrices y deformación en ambas extremidades inferiores, Daniels 1/5 en miembros pélvico izquierdo, Daniels 3/5 en miembro pélvico derecho, llenado capilar menor a dos segundos, sin edema.
En la valoración de vía aérea presenta apertura bucal grado II (2.7cm), Mallampati grado 2, Patil Andreti grado II (6cm), Bell House Dore grado I, distancia esternomentoniana clase III (12cm), protrusión mandibular grado I, dentinogénesis imperfecta, con puente fijo en arcada dentaria superior. Índice de predicción de intubación Díficil (IPID) de 10 puntos (discreta dificultad, no requiere de maniobras adicionales). Exámenes de laboratorio prequirúrgicos (QS4, ES6, tiempos de coagulación) dentro de parámetros normales. En la biometría hemática (BH) se observa discreta trombocitopenia (124,000/uL). Electrocardiograma (ECG) rítmico, frecuencia cardiaca de 60 lpm, eje a la izquierda, sin datos de isquemia o necrosis.
ASA II, riesgo tromboembólico calculado con escala de Caprini modificada alto (5 puntos), riesgo hemorrágico alto. RAQ E2B.
Figura 2. Radiografía AP de miembro pélvico, se muestra fractura y alteraciones en la densidad del hueso.
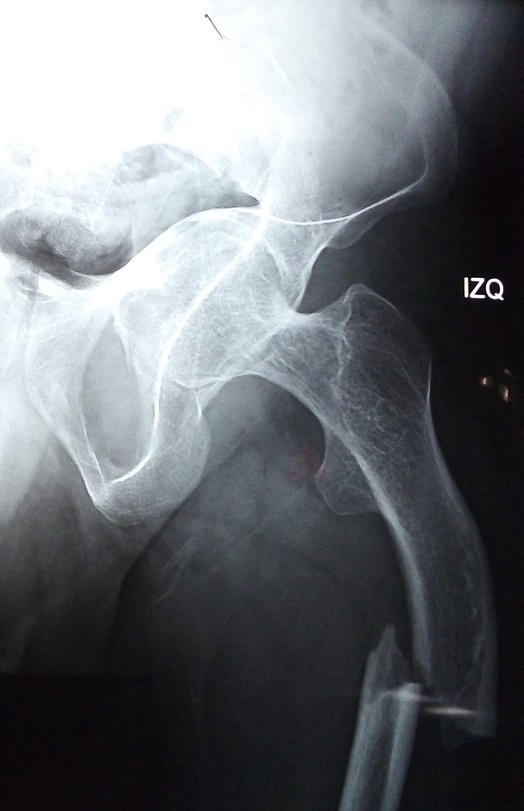
Se solicita un paquete globular y un plasma fresco congelado a disposición durante el trans anestésico.
A su llegada a quirófano se realiza monitorización básica no invasiva (tensión arterial, frecuencia cardiaca, saturación de oxígeno, electrocardiograma), con signos vitales normales, canalización vía venosa periférica #18 en miembro superior izquierdo.
Se cuenta con dispositivos supraglóticos de rescate en caso necesario.
Preoxigenación con mascarilla Facial con Fi02 100% por 3 minutos. Inducción anestésica con midazolam 0.03mg/Kg, fentanilo 5mcg/Kg, Propofol 2mg/Kg. Bloqueador neuromuscular cisatracurio 0.1mg/Kg. Intubación orotraqueal con laringoscopia directa al primer intento, Hoja MAC #3, Cormack Lehane 1, se coloca tubo Murphy #7.5fr, neumotaponamiento 6cc, comprobada ventilación simétrica bilateral, columna de aire y capnograma se fija a 22cm de la arcada dentaria.
Ventilación mecánica controlada por volumen, con los siguientes parámetros ventilatorios: volumen tidal 6ml/Kg peso, frecuencia respiratoria de 11 rpm, PEEP 7 cmH2O, I:E 1:2.
Mantenimiento anestésico balanceado, administrando CAM Sevoflurane 0.7. Hidratación con solución Hartman a temperatura ambiente, 850cc, balance de líquidos neutro. Hemodinámicamente estable.
Figura 3. Anatomía de paciente con OI.
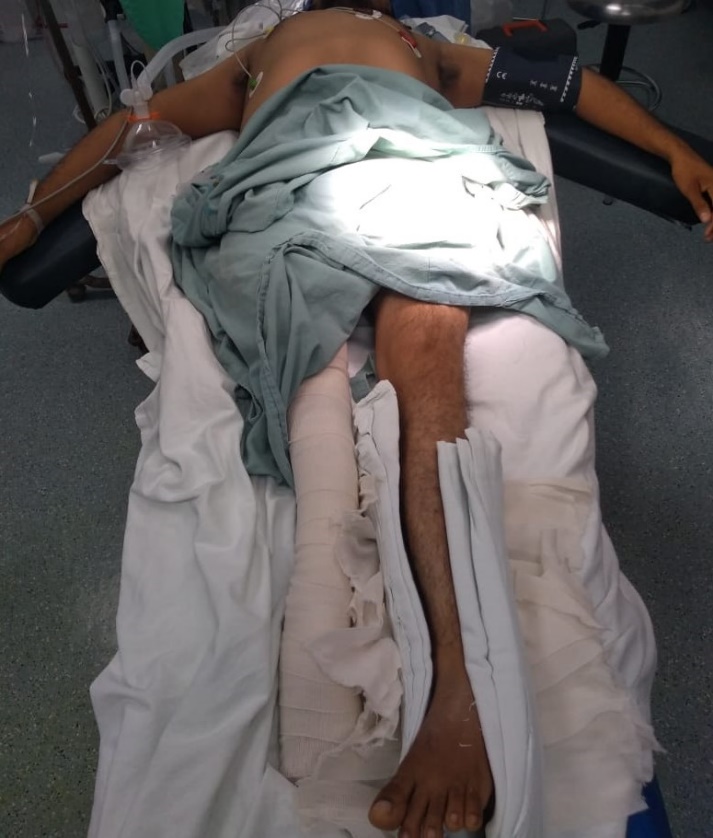
Medicación administrada durante el trans quirúrgico: analgesia basada en Ketorolaco 1mg/Kg, prevención de nausea y vómito posoperatorio con ondasetron 0.15mg/Kg.
Duración de procedimiento quirúrgico 100 min, sangrado 300mL, uresis no cuantificada. Una vez terminada la cirugía se descontinúa el anestésico inhalatorio, recuperada la mecánica ventilatoria y reflejos protectores de vía aérea íntegros, se procede a extubar, sin complicaciones
El paciente es transportado a la unidad de cuidados posanestésicos, donde es entregado al personal de dicha dependencia hemodinámicamente estable, con ventilación espontánea, Aldrete 9, Ramsay 2, EVA 0. Se reporta estable.
Durante todo el periodo perioperatorio, el paciente es manejado con precaución para evitar lesiones osteotendinosas y musculares. Fue dado de alta hospitalaria en su segundo día posoperatorio.
DISCUSIÓN
En los reportes bibliográficos se observa una mayor prevalencia de OI en el género masculino en pacientes intervenidos, con una edad que oscila entre 1 a 25 años, sin enfermedades asociadas en la mayoría, lo cual concuerda con la presentación de nuestro paciente (5,7,11).
La preparación adecuada y la evaluación preoperatoria son importantes, como es la elección de la técnica anestésica. La correcta identificación de factores de riesgo y la optimización de la salud antes de la cirugía, debe conducir a un curso de anestesia sin incidentes (7).
La implicación anestésica de la OI incluye intubación difícil relacionado a movilidad anormal de la columna cervical, dientes frágiles, luxación odontoaxial y resigo de fracturas mandibulares (5,7,11,12,18). Se ha reportado el uso exitoso de mascarilla laríngea, fibroscopio, fastrack y airtrack (9,18). Estos pacientes también presentan disfunción plaquetaria con un mayor riesgo de sangrado, anomalías cardiovasculares (6,7), tendencia a desarrollar hipertermia maligna y no maligna (8,9,15) y problemas con el posicionamiento del paciente debido a huesos frágiles (7, 9, 14,15, 16, 18), por lo que es importante disponer de hemoderivados, equipo para rescate la vía aérea, carro rojo y medidas para posicionamiento en caso necesario .
En paciente con diagnóstico de OI al administrar anestesia regional, se debe evaluar el perfil de coagulación debido al aumento asociado en el tiempo de sangrado a pesar del recuento normal de plaquetas, se encuentran casos de éxitos en la literatura a pesar del difícil abordaje por malformación en la columna (10-13).
Al menos el 50% de estos pacientes tienen niveles elevados de tiroxina sérica. La anestesia regional facilita la detección temprana de la tormenta tiroidea (18).
Respecto a la anestesia general, Karabiyik et al han recomendado TIVA, mientras que Malde et al han usado con éxito anestesia general balanceada (14- 16).
En nuestro caso se optó por anestesia general balanceada dadas las malformaciones en la columna que complicaban el abordaje regional así como la presencia de un IPID favorable.
Figura 4. Tórax en tonel en paciente con osteogénesis imperfecta.
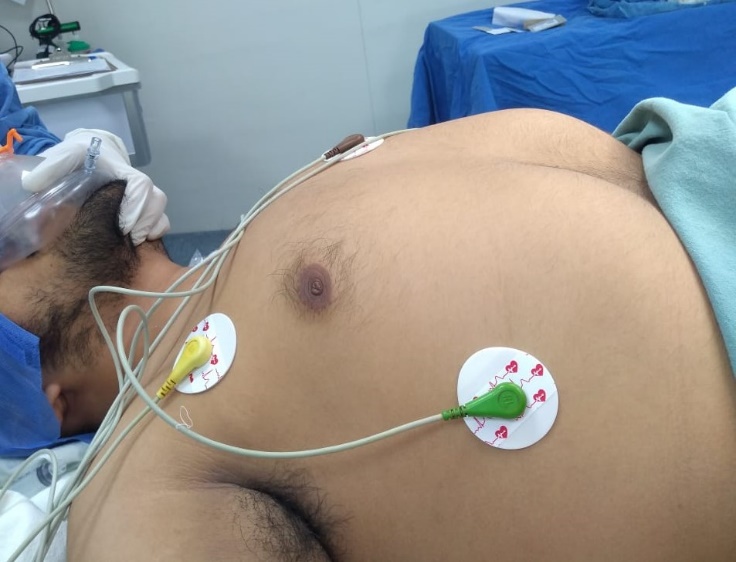
La cifoescoliosis asociada con alteraciones en la forma del tórax pueden disminuir la capacidad vital, con la hipoxemia arterial resultante debido a la falta de coincidencia de perfusión-ventilación, por lo tanto es importante preoxigenar adecuadamente al paciente y ajustar los parámetros ventilatorios de acuerdo a sus características , en la literatura se sugiere usos de PEEP en parámetros de 7-10cmH2O, como se utilizó con este paciente, con buena parámetros de CO2 espirado(10-13)
Se ha observado en estos pacientes tendencia a desarrollar hipertermia maligna y no maligna (8,9,15) .
La anestesia con sevoflurane es razonable con pacientes pediátricos con vía aérea difícil anticipada o acceso vascular difícil así como para mantenimiento de la anestesia en pacientes adultos (19, 20).
Durante la cirugía todos los puntos de presión deben estar bien acolchados y la colocación del paciente junto con el transporte debe ser delicada para evitar la aparición de nuevas fracturas (7, 9, 14-18), por lo que es importante una manipulación cuidadosa durante todo el trans anestésico para evitar fracturas agregadas.
Para el monitoreo de la presión arterial, los manguitos de presión sanguínea automatizados pueden ser peligrosos ya que el inflado excesivo puede provocar fracturas (14, 18), en nuestro paciente se modificaron los patrones de límite de insuflado para evitar lesiones agregadas.
CONCLUSIONES
Con el advenimiento de nuevas tecnologías en cuanto al diagnóstico y tratamiento en pacientes con osteogénesis imperfecta, cada vez se presenta un mayor número de reportes de pacientes con OI que se someten a cirugías de carácter electivo, por lo que resulta relevante plantearnos estrategias para el mejoramiento anestésico en estos pacientes.
La literatura presenta informes de casos exitosos de conductancia de cirugía bajo anestesia general en estos pacientes, con menores complicaciones respecto a técnicas regionales; sin embargo, es importante recordar que el manejo anestésico de la osteogénesis imperfecta impone un reto en el mantenimiento de la homeostasis por sus alteraciones asociadas: hematológicas, cardiacas, pulmonares, farmacocinéticas, vulnerabilidad durante el perioperatorio, manifestaciones esqueléticas adicionales e implicaciones en el manejo de la vía aérea. Por ello, es importante evaluar de forma integral al paciente, tomando en cuenta las condiciones basales para así elegir la técnica anestésica más adecuada.
REFERENCIAS
1. Marini JC, Cabral WA. Osteogenesis imperfecta. En: Thakker R, editor. Genetics of Bone Biology and Skeletal Disease. 2da Edición. London: Academic Press, Elservier (Internet). 2018 [citado 2019 Sep 21]; 397-420. Disponible en https://www.elsevier.com/books/genetics-of-bone-biology-and-skeletal-disease/thakker/978-0-12-804182-6
2. Moreta Colcha HE, Revelo Hidalgo EY, Borja Tapia PE, Vela Chasiluisa MA. Osteogénesis imperfecta. RECIMUNDO [En línea]; 2019 [citado 21 de septiembre de 2019];3(2):915-933. Disponible en: http://recimundo.com/index.php/es/article/view/483/558?fbclid=IwAR1cgvmlhQK5AU-k3Ld_Rf1YJkpCPI2t6PkHsmE2oTC8nDSapaEq7nPWTMI.
3. Barnes A, Chang W, Morello R, Cabral W, Weis M. Deficiency of cartilage-associated protein in recessive lethal osteogenesis imperfecta. N Engl J Med [En línea]. 2006 [citado 21 de septiembre de 2019]; 355(6): 2757-2764. Disponible en: https://www.nejm.org/doi/10.1056/NEJMoa063804?url_ver=Z39.88-2003&rfr_id=ori%3Arid%3Acrossref.org&rfr_dat=cr_pub%3Dwww.ncbi.nlm.nih.gov.
4. Cabral W, Chang W, Barnes A, Weis M. Prolyl 3-hydroxylase 1 deficiency causes a recessive metabolic bone disorder resembling lethal/ severe osteogenesis imperfecta. Nat Genet [En línea]. 2007 [citado 21 de septiembre de 2019]; 39(3): 359-365. Disponible en: https://www.nature.com/articles/ng1968.
5. Escribano Rey RJ, Duart Clemente J, Martínez de la Llana O. Osteogénesis imperfecta: tratamiento y resultado de una serie de casos. Rev Española de Cirugía Ortopédica y Traumatología 2014; 58 (2): 114-119.
6. Quelca-Choque HG, Bustamante-Cabrera G. Osteogénesis Imperfecta. Rev Act Clin Med [En línea]. 2014 [citado 21 de septiembre de 2019]; 45: 2394-2399. Disponible en: http://www.revistasbolivianas.org.bo/pdf/raci/v45/v45a08.pdf?fbclid=IwAR2es_zH5t9IAMp3pHJcNXkWMGXsYxrVECb5T6gfmB0OlaKiOtqCwb1cpXQ.
7. Barnuevo Cruz G, Cepeda Mora A. Caso de fractura de cúbito en niño con osteogénesis imperfecta, implicaciones anestésicas. Revista Médica-Científica CAMbios. 2019; 14(25): 66-68.
8. Stynowick G, Tobias JD. Perioperative Care of patient with osteogenesis imperfecta. Orthopedics [En línea]. 2007 [citado 21 de septiembre de 2019]; 30: 1044-1049. Disponible en: https://www.ncbi.nlm.nih.gov/pubmed/18198777.
9. Oakley T, Reece LP. Anesthetic implicactions for the patient with osteogenesis imperfecta. AANAJ 2010; 78: 47-53.
10. Errer Catasús T, León García A, Tey Pons M, Arenas Díaz AL, Marqués López F. Artroplastía total de cadera en osteogénesis imperfecta. A propósito de un caso. Acta ortop. mex [En línea]. 2017 [citado 21 de septiembre de 2019]; 31( 4 ): 202-205. Disponible en: http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S2306-41022017000400202.
11. Van Dijk FS, Sillence DO. Osteogenesis imperfecta: clinical diagnosis, nomenclature and severity assessment. Am J Med Genet A [En línea]. 2014 [Citado 21 de septiembre de 2019]; 164 (6): 1470-1481. Disponible en: https://www.ncbi.nlm.nih.gov/pubmed/24715559
12. Marini JC, Blisset AR. Nuevos genes en el desarrollo óseo: novedades en osteogénesis imperfecta. J Clin Endocrinol Metab 2013; 98: 3095 – 3103.
13. Radunovic Z , Wekre LL , Diep LM , Steine K . Anomalías cardiovasculares en adultos con osteogénesis imperfecta. Am Heart J 2011; 161 : 523 - 529 .
14. Warman ML , Cormier ‐ Daire V , Hall C , Cracovia D, Lachman R . Nosología y clasificación de los trastornos genéticos esqueléticos: revisión de 2010. Am J Med Genet Parte A 2011;155: 943 - 968.
15. Engel Espinosa W, Arrázola Cabrera B, Peralta Rodríguez P, García Molina C, Ortigosa Solórzano E. Experiencia en el tratamiento anestésico de los pacientes afectos de osteogénesis imperfecta. Rev Española de Anestesiología y Reanimación [En línea]. 2011 [Citado 21 de septiembre de 2019]. 58 (3): 151-155. Disponible en: https://www.elsevier.es/es-revista-revista-espanola-anestesiologia-reanimacion-344-articulo-experiencia-el-tratamiento-anestesico-los-S0034935611700226.
16. Munish G, Manish J, Amit G. Anaesthetic Management of A case of Osteogenesis imperfecta with urinary bladder Stone: A Case Report. Indian J Anaesth [En línea]. 2009 [Citado 21 de septiembre de 2019]; 53 (1): 68-70. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2900037/?report=classic&fbclid=IwAR0n3nIvyHQDr8Lu1K1cEsziS9PZAPFTfM4lZNRHWv7DV2k1-DQywcYBU08.
17. Karabiyik L, Parpucu M, Kurtipek O. Total Intravenous anaesthesia and the use of an intubating laryngeal mask in a patient with osteogenesis imperfecta. Acta Anestesiología Scand [En línea]. 2002 [Citado 21 de septiembre de 2019]. 46 : 618-19. Disponible en: https://www.ncbi.nlm.nih.gov/pubmed/12027862.
18. Gupta D, Purohit A. Anesthetic management in a patient with osteogenesis imperfecta for rush nail removal in femur. Anesth Essays Res [En línea]. 2016 [Citado 21 de septiembre de 2019].10:677-9. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5062238/.
19. Arzu K, Nilgün K, Ali S. Anesthesia Management in Rare case: osteogenesis imperfecta. British Journal of Pharmaceutical Research [En línea]. 2017 [Citado 21 de septiembre de 2019]. 15(5): 1-5. Disponible en: https://www.researchgate.net/publication/329075736_Anesthesia_Management_in_Rare_Case_Osteogenesis_Imperfecta.
20.Erdogan MA, Sanli M, Ersoy MO. Manejo de la anestesia en un niño con osteogénesis imperfecta y epidural hemorragia. Rev Bras Anestesiol [En línea]. 2013 [Citado 21 de septiembre de 2019]. 63 (4): 366-368. Disponible en: https://www.sciencedirect.com/science/article/pii/S2255496313000135





